Investigadores del CINN identifican factores clave en el desarrollo de un subtipo agresivo de tumor cerebral
El trabajo es fruto de la colaboración entre el Grupo de Epigenética del Cáncer y Nanomedicina del CINN-CSIC, del Instituto de Investigación Sanitaria del Principado de Asturias (ISPA) y el Instituto Universitario de Oncología del Principado de Asturias (IUOPA).
Los resultados obtenidos en este estudio revelan la existencia de proteínas clave en el desarrollo de un agresivo subtipo de glioblastoma, el mesenquimal.
La metodología empleada en la investigación abre la puerta a la identificación de nuevos factores reguladores en distintos tipos de escenarios y enfermedades que puedan ayudar a su tratamiento.
La revista internacional Molecular Oncology ha publicado recientemente un estudio en el que se identifican distintas proteínas cuyo papel podría ser fundamental en el avance del glioblastoma multiforme, en concreto, en el agresivo subtipo mesenquimal. Esta investigación ha sido realizada por el grupo de Epigenética del Cáncer y Nanomedicina, el cual se encuentra en el Instituto de Investigación Sanitaria del Principado de Asturias (ISPA) y vinculado al CINN-CSIC, IUOPA o la red CIBERER, estando coordinado por los investigadores Agustín Fernández Fernández y Mario Fernández Fraga.
El Gliobastoma y sus subtipos
El glioblastoma es un tumor agresivo que se origina en el sistema nervioso central, con una tasa de supervivencia muy baja, lo cual es debido principalmente al rápido crecimiento y avance de la enfermedad y a la ausencia de tratamientos médicos efectivos contra el mismo. En este sentido, en los últimos años se han realizado grandes avances a la hora de abordar el estudio del cáncer mediante la incorporación de técnicas moleculares para el diagnóstico y clasificación de pacientes oncológicos. Más recientemente se han comenzado a aplicar tecnologías de amplia resolución, –llamadas tecnologías ómicas–, que permiten estudiar desde una perspectiva global y con un alto grado de detalle las diferencias intrínsecas existentes entre pacientes que tienen el mismo tipo de tumor, lo que en el caso del glioblastoma ha permitido diagnosticar a pacientes en distintos subtipos, proneural, mesenquimal y clásico, los cuales exhiben un distinto comportamiento y agresividad en su avance.
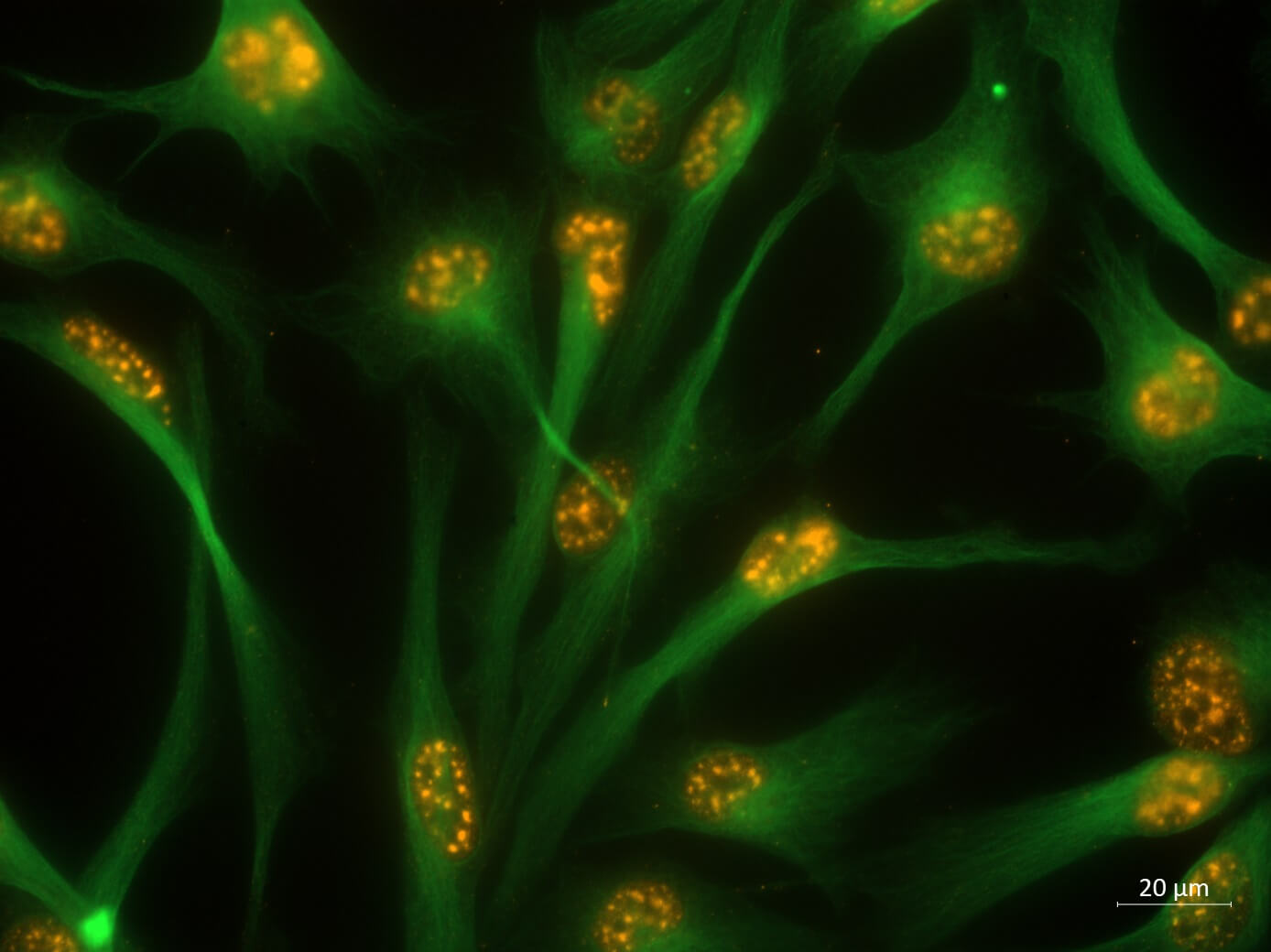
Imagen de una microscopía de fluorescencia de un cultivo de células madre de glioblastoma del subtipo mesenquimal derivadas de pacientes donde se observa la localización de la proteína SMAD3, la cual parece tener un rol clave en su desarrollo.
Una investigación que abre la puerta al tratamiento personalizado del Gliobastoma de subtipo mesenquimal
Por medio de este estudio, “buscamos realizar un enfoque integrativo, donde investigamos las diferencias que existen entre los distintos subtipos tumorales analizando las distintas capas de complejidad de la información celular, como son los patrones de metilación del ADN y de expresión génica”, argumenta Pablo Santamarina Ojeda, primer firmante del estudio. Por otro lado, su colega Juan Ramón Tejedor, co-primer firmante del trabajo apunta que “este enfoque nos ha permitido encontrar cómo distintas proteínas parecen tener un papel importante en el desarrollo del subtipo mesenquimal, por lo que podrían ser utilizadas como dianas terapéuticas en tratamientos personalizadas con pacientes que padecen este tipo de tumor.” En concreto, mediante el estudio de la metilación del ADN, los investigadores buscan “huellas” o “trazos” entre los distintos subtipos que les permitan identificar qué proteínas puedan estar activando rutas de señalización indispensables para el crecimiento tumoral.
En esta línea, Mario Fernández Fraga, profesor de investigación del CSIC y coordinador del estudio afirma que “la metodología utilizada en este estudio puede ser aplicada a distintas enfermedades de las cuales no conozcamos su etiología o cómo se encuentran dirigidas. De este modo, esto nos abre la puerta para estudiar en más detalle no sólo la segregación de los tumores en distintos subtipos, mejorando así el manejo de la enfermedad, sino la búsqueda de potenciales dianas terapéuticas que nos permita diseñar un tratamiento más eficaz”. Ampliando las palabras de su homólogo, Agustín Fernández Fernández, científico titular del CSIC, aporta que “es un paso adelante, pero debemos ser precavidos. A pesar de haber comprobado in vitro el efecto de la inhibición de estos factores en un modelo de estudio sofisticado utilizando células derivadas de distintos subtipos de glioblastoma, es necesario continuar con la investigación y ampliar el estudio hacia modelos in vivo más complejos, en los cuales sabremos el futuro potencial de las terapias dirigidas contra estas proteínas”.

De izquierda a derecha: Pablo Santamarina Ojeda, Mario Fernández Fraga, Agustín Fernández y Juan Ramón Tejedor
Acerca de la investigación
Esta investigación ha podido llevarse a cabo con la financiación del Gobierno del Principado de Asturias a través de los programas GRUPIN; de la Asociación Española Contra el Cáncer (AECC); del CSIC, por medio de la Plataforma Temática Interdisciplinar de Salud Global; del Ministerio de Ciencia e Innovación gracias a su programa de Recuperación, Transformación y Resiliencia, y al Instituto de Salud Carlos III por la subvención de los distintos proyectos FIS. Además, los investigadores que han participado en este estudio son financiados a través de distintas entidades como el IUOPA, CSIC e ISPA.
Referencia del trabajo: Pablo Santamarina-Ojeda, Juan Ramón Tejedor, Raúl F. Pérez, Virginia López, Annalisa Roberti, Cristina Mangas, Agustín F. Fernández, Mario F. Fraga. Multi-omic integration of DNA methylation and gene expression data reveals molecular vulnerabilities in glioblastoma. Molecular Oncology. 2023. https://doi.org/10.1002/1878-0261.13479