Centros de investigación de toda España colaboran para desplegar las últimas tecnologías de análisis genómico e identificar dianas terapéuticas en cáncer infantil
- El estudio, fruto de la colaboración multicéntrica, desentraña vulnerabilidades moleculares de las leucemias pediátricas agudas desde múltiples perspectivas, por primera vez.
- Los resultados se basan en la secuenciación del genoma, epigenoma y transcriptoma completo de 69 bebés con un tipo de leucemia de mal pronóstico y su análisis computacional.
- La investigación fue liderada por investigadores del Instituto de Investigación contra la Leucemia Josep Carreras, el Centro de Investigación en Nanomateriales y Nanotecnología (CINN-CSIC) y el Instituto de Investigación Sanitaria del Principado de Asturias (ISPA).
La prestigiosa revista The Journal of Clinical Investigation (JCI), acaba de publicar una investigación centrada en la identificación de alteraciones moleculares en leucemias pediátricas agudas que podrían actuar como pilares indispensables para sustentar la proliferación tumoral.
Esta investigación, de marcado carácter internacional, ha sido liderada por el grupo de Biología de células madre, leucemia del desarrollo e inmunoterapia del Instituto de Investigación contra la Leucemia Josep Carreras y el grupo de Epigenética del Cáncer y Nanomedicina del Instituto de Investigación Sanitaria del Principado de Asturias (ISPA-CSIC).
“La importancia clínica del trabajo radica en la magnitud y el carácter multidisciplinar del estudio, ya que todos los niños pertenecen al prestigioso protocolo internacional de tratamiento para leucemias en bebes, INTERFANT, lo que hace que las asociaciones clínicas sean muy fiables”, asegura Pablo Menéndez, jefe del grupo de Biología de células madre, leucemia del desarrollo e inmunoterapia del Instituto de Investigación Josep Carreras.
Gracias a un esfuerzo colaborativo entre distintas instituciones nacionales e internacionales, los investigadores han podido secuenciar el genoma, el epigenoma y el transcriptoma de 69 bebés con un tipo de leucemia de mal pronóstico. “Curiosamente, estas leucemias pediátricas cursaban con un número muy pequeño de mutaciones, lo que nos llevó a explorar diferentes aproximaciones para identificar posibles dianas terapéuticas, o talones de Aquiles del tumor”, prosigue Menéndez.
Para ello, el laboratorio de Epigenética del Cáncer y Nanomedicina ha empleado una batería de análisis computacionales con el fin de delinear el mapa de alteraciones moleculares existente en estas leucemias pediátricas. “Mediante el empleo de tecnologías -ómicas (genómica, transcriptómica y proteómica) de última generación, hemos podido caracterizar con gran detalle el epigenoma y el transcriptoma de ciertos tipos de leucemias pediátricas agudas. La novedad de este estudio radica en la integración de dichos datos, que nos ha permitido vislumbrar, de una manera mucho más precisa, las rutas de señalización sobre las que se sustenta este tipo de cáncer”, comenta Juan Ramón Tejedor, primer firmante del artículo.
Por otra parte, Agustín Fernández, científico titular del CINN-CSIC y también miembro del laboratorio de Epigenética del Cáncer y Nanomedicina del ISPA, incide en que “existen numerosas similitudes entre los distintos tipos de leucemias pediátricas que analizamos. Sin embargo, nos llamó la atención el marcado efecto funcional del complejo transcripcional AP-1 en aquellas leucemias con peor prognosis, lo que nos llevó a profundizar sobre el posible papel de estos factores en la proliferación tumoral”.
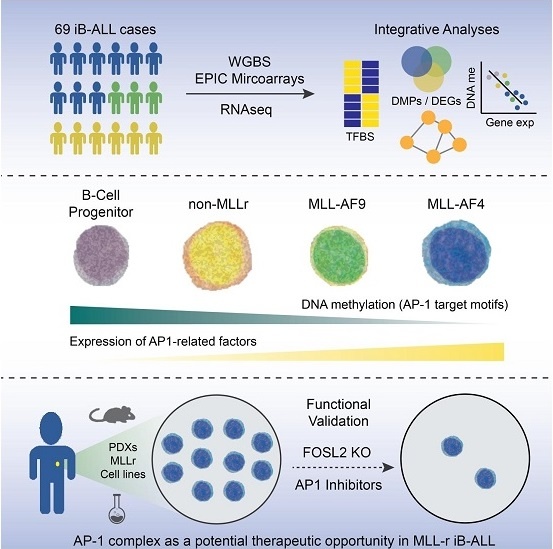
La veracidad de estas observaciones obtenidas in silico, es decir, por medios computacionales, ha sido confirmada de manera exhaustiva por investigadores del Instituto de Investigación Josep Carreras. Clara Bueno, coautora principal del trabajo, explica que “Hemos desarrollado una serie de sofisticados ensayos in vitro, ex-vivo e in-vivo para validar el efecto de la vía de AP-1 en este tipo de leucemias pediátricas”. Para ello, los investigadores utilizaron una serie de técnicas experimentales que incluyen modelos de edición genética mediadas por la tecnología CRISPR, modelos animales de xenotransplante con células de pacientes, ensayos con inhibidores farmacológicos e incluso un modelo de quimioterapia en ratón a la carta, que les permitió demostrar el potencial efecto terapéutico de este complejo transcripcional en modelos de ratón, paso previo a la experimentación en pacientes humanos.
Estos resultados abren la posibilidad de desarrollar nuevos ensayos clínicos para determinar el efecto de inhibidores farmacológicos de determinadas rutas de señalización en cáncer infantil. En este aspecto, Mario Fernández Fraga, coordinador del laboratorio de Epigenética del Cáncer y último co-firmante del artículo, comenta que “estos resultados son muy prometedores, pero hay que ser cauteloso y recordar que todavía nos encontramos en fases preliminares de investigación en modelos animales”.
Además de las instituciones anteriormente mencionadas, en este estudio también han colaborado otras entidades españolas como la Universidad de Oviedo, el Instituto Universitario de Oncología del Principado de Asturias (IUOPA) y los Centros de Investigación Biomédica en Red de Enfermedades Raras (CIBERER) y Cáncer (CIBERONC), el Instituto de Biomedicina y Biotecnología de Cantabria (IBBTEC), el Centro Nacional de Investigaciones Oncológicas (CNIO), la Universidad de Barcelona y el Hospital Infantil Universitario Niño Jesús. A nivel internacional, se ha contado con la participación del centro de Investigación Tettamanti (Italia), el Hospital Armand Trousseau (Francia) y el centro de Oncología pediátrica Princess Maxima (Holanda).
Financiación
Este estudio ha podido desarrollarse gracias a la financiación de diversas entidades y fundaciones, entre las que destacan el European Research Council (ERC), el Ministerio de Economía y Competitividad (MINECO), el Instituto de Salud Carlos III (ISCIII), el Plan de Ciencia, Tecnología e Innovación del Principado de Asturias (PCTI), la Asociación Española Contra el Cáncer (AECC), la Fundación UnoEntreCienmil, la Fundación General CSIC y la Fundación Leo Messi, entre otras.
Más información
“Integrative methylome-transcriptome analysis unravels cancer cell vulnerabilities in infant MLL-rearranged B-cell acute lymphoblastic leukemia”. https://www.jci.org/articles/view/138833